分岔或失稳现象常常发生在细胞生物学中,如上皮细胞喷出、肌动蛋白诱导的膜起泡、粘附细胞的多态性和微丝微管的屈曲,这些对发育和病理学至关重要。突跳不稳定性是系统平衡状态之间响应小扰动的快速转变行为,与细胞活动不同状态/功能的触发有关。例如,实体瘤细胞的转移可能由肿瘤微环境中的静水压力学因素引起。因此,我们探讨了粘附细胞的突跳失稳是否有可能是由生长中的肿瘤特有的静水压力变化引起的。
细胞体积和形态调节影响粘附细胞的多种行为,如增殖、迁移和跨上皮运输等,并且可能由离子和水通过细胞膜的运输有关。一般情况下,细胞体积调节是稳态的,但在一些情况下,它会随着静水压力的大小而变化。例如随着某些癌症的发展,静水压影响细胞生理学和病理生理学肿瘤微环境,细胞对静水压的体积反应可能存在显著差异:悬浮的K562和HL60白血病细胞的体积随着静水压的增加而减少,而粘附的CL1-5和A549肺癌细胞则相反。
为了理解这种差异,我们开发了一个静水压调控的粘附细胞力学模型(图1),将静水压力的变化与粘附细胞的粘附状态联系起来,同时考虑了细胞粘附能量密度和静水压力对控制细胞体积的离子通道动力学的影响,研究在静水压力下作用下粘附力、膜张力和几何约束如何协同控制细胞形态和体积。该模型预测了在一定范围的粘附能量密度下粘附细胞形态在静水压力作用下的双稳态,即从粘附状态到脱粘附状态的突跳不稳定性。我们进一步预测,在临界静水压力下,粘附细胞将发生突跳不稳定性从基底“跳起来”,而越过该不稳定性,粘附细胞的体积对静水压力相对不敏感。该研究揭示了在静水压力扰动下癌细胞转移的潜在机制,建立的模型为癌细胞转移的风险评估提供的理论基础。
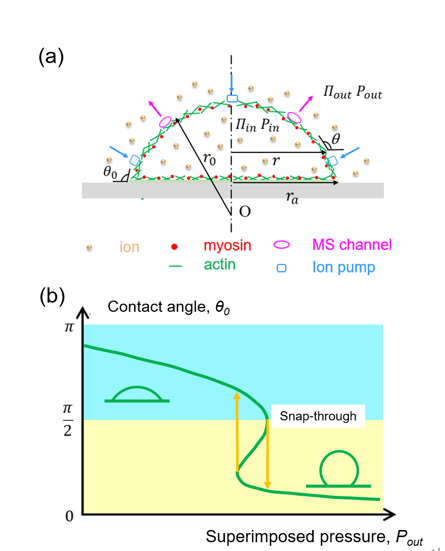
图1 静水压调控的粘附细胞力学模型和突跳不稳定性
近日,题为“A Snap-Through Instability of Cell Adhesion Under Perturbations in Hydrostatic Pressure”发表在国际固体力学旗舰期刊Journal of the Mechanics and Physics of Solid(JMPS)。论文的第一作者为南京航空航天大学刘少宝副教授,共同第一作者为西安交通大学本科生杨海谦、西安交通大学徐光魁教授,通讯作者为西安交通大学徐峰教授,共同通讯作者为南京航空航天大学卢天健教授。其他作者包括南京航空航天大学本科生武靖博、西安交通大学硕士生陶如、王蒙博士、何榕晏博士、南京航空航天大学韩玉龙教授、美国圣路易斯华盛顿大学Guy Genin教授,专业领域涵盖力学、力学生物学、力医学等。该工作得到了国家自然科学基金杰出青年基金、重点项目、面上项目等的支持。
论文链接:https://doi.org/10.1016/j.jmps.2023.105476